Waarom zit het hart links en de lever rechts?
In een gezond menselijk lichaam zit het hart links en de lever rechts. Verrassend genoeg zitten bij sommige mensen deze organen andersom in hun lichaam. Deze normale of abnormale asymmetrie is terug te voeren op de tijd dat je een embryo was. In de eerste dagen van je ontwikkeling vormt zich op je embryo een kleine, met vloeistof gevulde holte die de embryonale knoop wordt genoemd. Binnenin creëren kleine microhaartjes, die trilharen worden genoemd, een stroompatroon dat bepaalt waar organen in je lichaam groeien. De wetenschap achter dit stromingsproces is tot nu toe een mysterie gebleven. Onderzoekers van de Technische Universiteit Eindhoven (TU/e) en de Rijksuniversiteit Groningen (RUG) hebben belangrijke details achter dit proces onthuld door als eerste ter wereld een kunstmatige embryonale knoop te bouwen. In deze kunstmatige embryonale knoop wordt via synthetische, magnetisch gestuurde cilia een stroompatroon gegenereerd. Via geavanceerde simulaties is onderzocht wat er in de knoop gebeurt. De resultaten van dit onderzoek zijn gepubliceerd in het wetenschappelijke tijdschrift Science Advances.
FSE Science Newsroom | Tekst TU/e
Aan de buitenkant is het menselijk lichaam bilateraal symmetrisch. Een gezicht met twee ogen en twee oren die elkaar spiegelen. Ledematen die hetzelfde doen. Binnen in het lichaam is het een ander verhaal. Hoewel gepaarde organen, zoals longen en nieren, ongeveer bilateraal symmetrisch zijn, geldt dat niet voor de andere organen. We hebben geen twee harten of twee levers. Bovendien vind je deze organen aan tegenovergestelde kanten van het lichaam – het hart aan de linkerkant en de lever aan de rechterkant.

Embryonale oorsprong
‘Het is helemaal terug te voeren tot de eerste embryonale fase’, zegt Jaap den Toonder, hoogleraar bij de faculteit Mechanical Engineering en hoofd van de Microsystems-onderzoeksgroep bij de TU/e. ‘Het heeft te maken met wat er gebeurt in wat een embryonale knoop wordt genoemd.’ De embryonale knoop is een kleine holte die een vloeistof bevat (water met eiwitten, hormonen en andere stoffen). De bovenkant wordt afgesloten door een membraan, terwijl de onderste laag is bekleed met enkele honderden kleine microhaartjes die trilharen (cilia) worden genoemd. De hele knoop is slechts een paar honderd micrometer breed.
‘De cilia in de embryonale knoop draaien in dezelfde richting en maken een gekantelde kegelvormige beweging. Dit genereert een vloeistofstroom in de knoop tegen de klok in. We weten dat deze stroming een sleutelrol speelt in de links-rechtssymmetrie', legt Den Toonder uit
Een cruciale vraag die echter onbeantwoord blijft, is hoe de stroming de links-rechtsverdeling van organen in het lichaam precies in gang zet. Om deze vraag te beantwoorden, leidde hij een project om een wereldprimeur te ontwerpen – een kunstmatige embryonale node. Tanveer ul Islam, Yves Bellouard (universitair hoofddocent aan het Zwitserse EPFL) en Den Toonder waren verantwoordelijk voor de ontwikkeling van de kunstmatige embryonale knoop. Ishu Aggarwal en Patrick Onck, beiden verbonden aan de RUG, leidden de ontwikkeling van een model om de embryonale knoop te simuleren.
Zorgvuldig fabricageproces
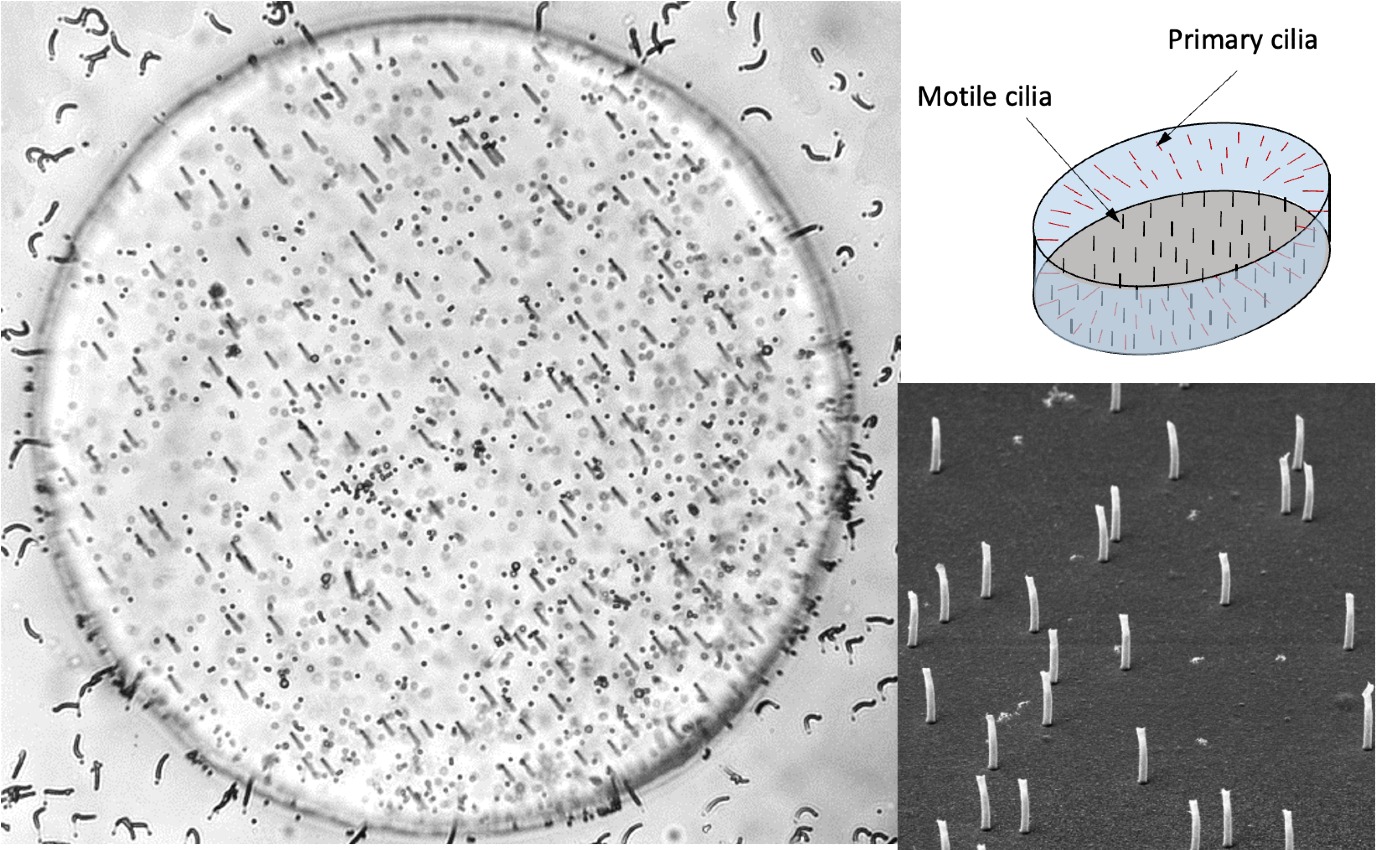
‘Het ontwikkelen van de kunstmatige embryonale knoop omvatte twee belangrijke microfabricageprocessen’, zegt Tanveer ul Islam. 'In het eerste proces maakten we de cilia van een uniek magnetisch polymeermateriaal dat werd ontwikkeld in het MicrofabLab van TU/e. Het tweede proces betrof het maken van de knoop zelf.
Hoewel de kunstmatige embryonale knoop ongeveer vijf keer groter is dan een echte embryonale knoop (ongeveer 500 micrometer doorsnede), heeft ze nog steeds een lengteschaal die vergelijkbaar is met die van een echte embryonale knoop. ‘De reden voor deze grootte is dat de lichtmicroscoop de beweging van alle cilia en de vloeistof niet nauwkeurig zou kunnen visualiseren als de knoop kleiner was’, vertelt Tanveer ul Islam, die het grootste deel van dit werk uitvoerde.
Vervolgens ontwierp Tanveer ul Islam met zijn collega's een manier om de magnetische cilia te bewegen, terwijl ze tegelijkertijd het stroompatroon dat binnen de knoop ontstond observeerden. ‘We ontwikkelden een nieuwe magnetische methode om de beweging van de trilhaartjes te sturen. We hebben deze methode ook laten patenteren. Met behulp van kleine oplichtende deeltjes konden we de vloeistofstroom heel precies filmen. Zonder deze visualisatiemethode zouden wij niet in staat zijn geweest om te achterhalen hoe de embryonale knoop functioneert,’ aldus Tanveer ul Islam. De visualisaties lieten zien hoe de cilia de stroming in de cel starten en zeer specifieke stromingspatronen veroorzaken.

Twee mechanismen die samenwerken
Hij vervolgt: ‘Er bestaan verschillende hypotheses om uit te leggen hoe asymmetrie ontstaat. Eén hypothese stelt dat de cilia aan de onderkant de stroming veroorzaken. Andere cilia, die niet kunnen bewegen, ook wel primaire cilia genoemd en gelegen aan de randen van de knoop, voelen vervolgens de sterkte van die stroming doordat ze vervormen. Dit activeert op zijn beurt een genetisch programma dat de ontwikkeling van asymmetrische organen aanstuurt. Een andere hypothese is dat dit genetische programma juist wordt gestart doordat de nodale stroom binnen de knoop zorgt voor een ongelijke verdeling van morfogenen, de signaalmoleculen die de ontwikkeling sturen.’
Om deze hypotheses te testen met behulp van de stromingspatronen die in de kunstmatige embryonale knoop werden gemeten, was het numerieke model van Ishu Aggarwal en Patrick Onck van de Rijksuniversiteit Groningen van groot belang. ‘Jaap en ik werken al meer dan twintig jaar samen aan onderzoek naar kunstmatige magnetische trilhaartjes,’ zegt Onck. De combinatie van de experimenten en de simulaties liet zien dat beide mechanismen, het buigen van de primaire cilia én de verdeling van morfogenen, samenwerken. Dit wijst erop dat er een synergie bestaat tussen deze twee systemen die samen de links‑rechtsasymmetrie in de orgaanontwikkeling aansturen.

Gecombineerde aanpak
Tot nu toe was het geen enkele onderzoeksgroep gelukt om de hele embryonale knoop te simuleren, omdat bestaande modellen te veel rekenkracht nodig hebben. ‘Om de vloeistofstroom in de embryonale knoop te simuleren, hebben we de cilia gemodelleerd als stijve staafjes. Deze volgden precies het veranderende magnetische veld dat we in de experimenten gebruikten. Door de cilia op de gemeten plekken te zetten, konden we het stromingspatroon uit de experimenten goed nabootsen’, licht Onck toe.
De Groningse onderzoekers gebruikten een zelfgemaakt algoritme om de simulaties eenvoudiger te maken. ‘We maakten een set vergelijkingen waarmee we de stroming konden berekenen binnen een redelijke tijd. Toch duurden de simulaties nog maanden op onze supercomputers,’ legt Onck uit.
‘Het belangrijkste is dat we niet alleen de stroming hebben gesimuleerd, maar ook hoe morfogenen zich in de knoop verspreiden en hoe de primaire cilia vervormen. Samen met de experimenten was deze gecombineerde aanpak nodig om te laten zien wat de links-rechtsasymmetrie veroorzaakt: de samenwerking tussen beide mechanismen.’
Referentie: Tanveer ul Islam, Ishu Aggarwal, Yves Bellouard, Patrick R. Onck, and Jaap M. J. den Toonder: Artificial embryonic node elucidates the role of flow in left-right symmetry breaking in vertebrates. Science Advances 25 maart 2026
