Simpel experiment wijst nieuwe weg voor zwavel-chemie
Het is verrassend eenvoudig om thiolen, het zwavelhoudende equivalent van alcoholen, te oxideren met een enzym. Dit ontdekten biochemici van de Rijksuniversiteit Groningen en Wageningen Universiteit, onafhankelijk van elkaar. Zij publiceerden hun vondst afgelopen vrijdag gezamenlijk in Angewandte Chemie, een van de belangrijkste tijdschriften voor chemisch onderzoek. De vondst kan een nieuwe manier opleveren om stankoverlast te verminderen.

‘Het onderzoek begon toen we de activiteit onderzochten van HMFO, een nieuw oxiderend enzym dat we onlangs hebben beschreven’, vertelt hoogleraar biochemie aan de RUG Marco Fraaije. HMFO kan van een reeks verbindingen de alcoholgroepen oxideren. ‘Een thiol groep lijkt in zekere zin op een alcohol, waarbij een zuurstofatoom is vervangen door zwavel. Daarom leek het de moeite waard te proberen of HMFO ook thiolen kon oxideren.’
Willem Dijkman, promovendus in de goep van Fraaije, deed de experimenten. ‘Het werkte meteen’, zegt hij. ‘Toen we het enzym toevoegden aan een verbinding met een thiol groep zagen we dat er direct zuurstof werd verbruikt. Dit wijst erop dat het enzym de verbinding inderdaad oxideert. Het was een heel simpel experiment. Maar het was een stuk moeilijker om uit te zoeken wat voor reactie er nu precies plaatsvindt.’
Bijzonder
Ondertussen waren collega’s van Fraaije en Dijkman aan de Wageningen Universiteit op hetzelfde spoor terecht gekomen, maar bij hen gebeurde dat per ongeluk. Zij probeerden een enzym dat alcoholen oxideert te beschermen in een oplossing door er een verbinding met een thiol groep aan toe te voegen. Dat zou oxidatieve stress door te hoge activiteit moeten voorkomen. Het oxiderende enzym is geel wanneer het in rust is, en rood bij activiteit. De onderzoekers uit Wageningen zagen dat de kleur veranderde na toevoeging van thiol en ontdekten al snel dat hun enzym deze groep kan oxideren.
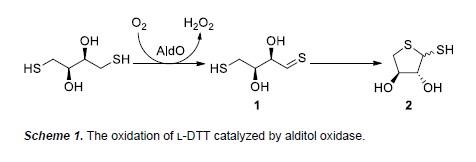
‘We werken nauw samen met deze groep, dus we hoorden al snel van elkaars resultaten’, vertelt Fraaije. ‘Dus besloten we om dit gezamenlijk te publiceren.’ Het artikel verscheen op 3 oktober in Angewandte Chemie, een van de belangrijkste vakbladen voor chemici. In dit artikel beschrijven ze hoe de enzymatische oxidatie van thiolen precies plaatsvindt.
Maar wat is er nu zo bijzonder aan een enzyme dat thiolen kan oxideren? Fraaije: ‘Allereerst, niemand wist nog dat die enzymen deze reactie kunnen uitvoeren. Naast HMFO hebben we nog drie andere oxiderende enzymen getest, en die konden hetzelfde kunstje.’ Daarnaast bevestigt deze ontdekking dat enzymen niet altijd zo specifiek zijn als we ooit dachten. ‘Deze enzymen maken geen onderscheid tussen alcoholen en thiolen.’
Stankoverlast
Een tweede bijzonder punt is dat de oxidatie een nogal reactieve verbinding oplevert met een thioaldehyde-groep, een zwavelatoom dat via een dubbele binding aan het molecuul vast zit. Deze verbinding is mogelijk een goed beginpunt voor het uitvoeren van verdere biochemische stappen, aangezien thioaldehyde veel reactiever is dan het vergelijkbare aldehyde (een zuurstof atoom dat via een dubbele binding vast zit).

Een laatste interessant punt is dat thiolen berucht zijn omdat ze soms onderdeel zijn van stinkende verbindingen. ‘De smerige stinkende vloeistof waarmee een stinkdier zijn vijanden afschrikt is gebaseerd op thiol-verbindingen’, weet Fraaije. Aan de andere kant, ook het rijke aroma van koffie wordt veroorzaakt door thiolen. Dus zou een thiol-oxiderend enzym mogelijk nuttig kunnen zijn voor het oplossen van stankoverlast of het aanpassen van het koffie-aroma.
Fraaije: ‘We moeten nu afwachten hoe de biochemische gemeenschap reageert op deze vinding en welke ideeën daaruit voortkomen. Een vergelijkbare ontdekking van een enzym dat amines kan oxideren heeft een heleboel nieuwe chemie opgeleverd en er is zelfs een bedrijf voor opgericht waar nu tientallen chemici werken. Dus wie weet wat er nog gaat gebeuren!’
Referentie: The Oxidation of Thiols by Flavoprotein Oxidases: a Biocatalytic Route to Reactive Thiocarbonyls. Tom A. Ewing, Willem P. Dijkman, Prof. Dr. Jacques M. Vervoort, Marco W. Fraaije and Prof. Dr. Willem J. H. van Berkel. Angewandte Chemie DOI: 10.1002/ange.201407520
| Laatst gewijzigd: | 01 juni 2020 10:23 |
Meer nieuws
-
16 april 2024
RUG ondertekent Barcelona Declaration on Open Research Information
De Rijksuniversiteit Groningen heeft de Barcelona Declaration on Open Research Information (Verklaring Open Onderzoeksinformatie) officieel ondertekend. Dit wordt gezien als een grote stap richting verantwoordelijke onderzoeksbeoordeling en open...
-
02 april 2024
Vliegen op houtstof
In Makers van de RUG belichten we elke twee weken een onderzoeker die iets concreets heeft ontwikkeld: van zelfgemaakte meetapparatuur voor wetenschappelijk onderzoek tot kleine of grote producten die ons dagelijks leven kunnen veranderen. Zo...
-
18 maart 2024
VentureLab North helpt onderzoekers op weg naar succesvolle startups
Het is menig onderzoeker al overkomen. Tijdens het werken vraag je je opeens af: zou dit niet ontzettend nuttig zijn voor de mensen buiten mijn onderzoeksveld? Er zijn allerlei manieren om onderzoeksinzichten te verspreiden. Denk bijvoorbeeld aan...

