Stofwisseling dirigent van de celdeling
Alle leerboeken vertellen dat de cyclus van groei en deling van cellen met een celkern wordt geregeld door het cycline-afhankelijke kinasecomplex. Maar RUG-onderzoekers hebben ontdekt dat metabole oscillaties optreden als de ‘dirigent’ van de celdeling. De resultaten zijn op 15 december 2016 gepubliceerd op de website van het tijdschrift Molecular Cell.
Cellen volgen een cyclus van DNA-duplicatie, groei en celdeling. Daarvoor is een nauwkeurige afstemming van processen in de cel nodig, zoals bij de ‘checkpoints’ die voorkomen dat cellen gaan delen als er iets - bijvoorbeeld met het gedupliceerde DNA - niet in orde is. Onderzoek wees uit dat het cycline-afhankelijke kinasecomplex deze cyclus reguleert. Voor deze ontdekking is in 2001 de Nobelprijs voor fysiologie of geneeskunde toegekend.
Niet hele verhaal
‘Maar er zijn aanwijzingen dat dit niet het hele verhaal is’, zegt RUG-systeembioloog Matthias Heinemann. Eén zo’n aanwijzing was dat cellen gewoon kunnen delen wanneer onderdelen van het cycline-afhankelijke kinase complex zijn verwijderd. Heinemann bedacht dat oscillaties in de stofwisseling mogelijk de maat van de celdeling bepalen. ‘We wisten dat de stofwisseling vaak synchroon oscilleert met de celcyclus. Dus misschien was dit een apart controlemechanisme.’
Onder de microscoop
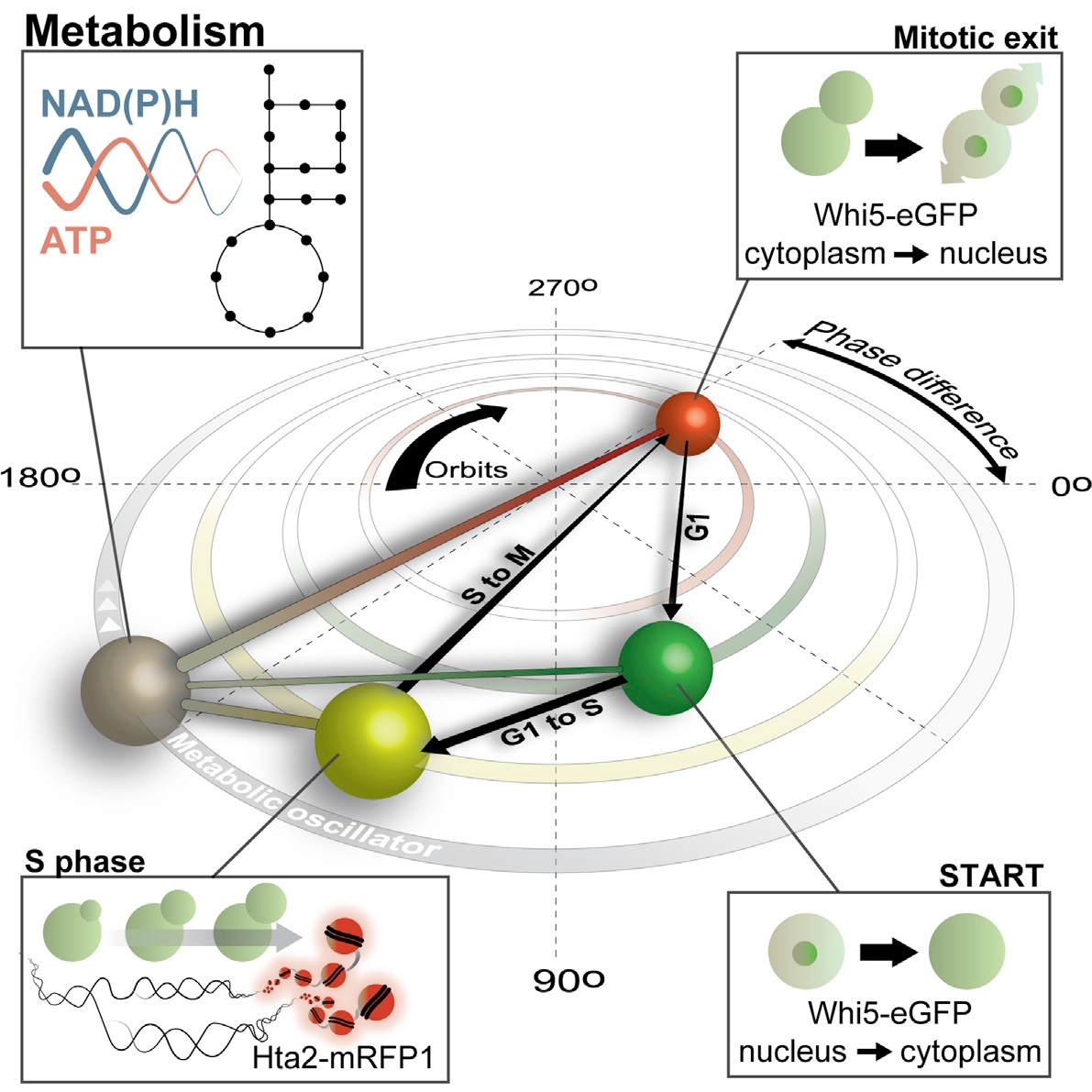
Heinemann onderzocht dit in gistcellen die in microscopisch kleine kanaaltjes werden gekweekt. Met deze methode is het mogelijk om individuele cellen dagenlang onder de microscoop te bestuderen. Met behulp van fluorescentie was het mogelijk twee indicatoren van de stofwisseling te meten: de elektronendrager NADH en de energiedrager ATP. Deze moleculen vertonen een oscillerend patroon, in een ritme dat doorgaans synchroon loopt met de celcyclus. Heinemann: ‘Maar we zagen soms cellen die niet deelden, terwijl ze wel de oscillaties in de stofwisseling vertoonden.’
Orkest en dirigent
De stofwisseling bleek een oscillator die onafhankelijk is van de celcyclus en die sneller gaat wanneer de cellen goed doorvoed zijn. Bij slechte voeding vertraagt de snelheid. ‘Wij betogen dat de stofwisseling en het cycline-afhankelijke kinase complex gekoppelde oscillatoren zijn, die samen de groei en deling van eukaryotische cellen [met een celkern, red.] reguleren.’ In andere woorden: het cycline-afhankelijke kinasecomplex is het orkest, terwijl de oscillaties van de stofwisseling als een dirigent het ritme bepalen.
Ontkoppeld
‘Maar als het metabolisme te snel of te traag gaat, kan de celcyclus het niet bijhouden’, zegt Heinemann. Beide oscillaties hebben een eigen natuurlijke frequentie. Onder normale omstandigheden zijn de twee oscillaties gekoppeld, ze nemen dan een gezamenlijke compromis-frequentie aan die het celdelingsproces bepaalt. Experimenten lieten zien dat de oscillaties van de stofwisseling en de celdeling inderdaad ontkoppeld kunnen raken.
Kijk bijstellen
Biologen zullen hun kijk op de regulatie van de celcyclus moeten bijstellen, denkt Heinemann: ‘De huidige visie is te smal en kan bijvoorbeeld niet verklaren waarom de celdeling door gaat als een deel van het cycline-afhankelijke kinase complex is verwijderd.’ Een belangrijke rol voor de stofwisseling is ook aannemelijk vanuit evolutionair perspectief: ‘Je verwacht dat de vroegste cellen of proto-cellen een simpel controlesysteem hadden om de deling te reguleren. Dan is de stofwisseling een voor de hand liggende kandidaat.’
Tumoren remmen
Dit nieuwe perspectief kan uiteindelijk ook belangrijk zijn voor de geneeskunde. ‘De meeste tumorcellen hebben een sterk verhoogde stofwisseling. Ingrijpen in de stofwisseling zou een manier kunnen zijn om de celdeling van tumoren te remmen.’
Meer informatie
- Referentie: Alexandros Papagiannakis, Bastian Niebel, Ernst C. Wit, and Matthias Heinemann: “Autonomous Metabolic Oscillations Robustly Gate the Early and Late Cell Cycle.” Molecular Cell, December 15, 2016, DOI 10.1016/j.molcel.2016.11.018
| Laatst gewijzigd: | 14 april 2020 10:51 |
Meer nieuws
-
23 april 2024
Negen MSCA Doctoral Network subsidies voor FSE onderzoekers
Negen onderzoekers van de Faculty of Science and Engineering hebben een Horizon Europe Marie Sklodowska Curie Doctoral Network subsidie ontvangen.
-
22 april 2024
Charissa Roossien ontvangt JTF-subsidie voor ontwikkelen Health Tracker
Dr. Charissa Roossien (ENTEG) heeft met succes een Just Transition Fund (JTF) subsidie van 1,8 miljoen euro binnengehaald voor de ontwikkeling van een Health Tracker voor betrouwbare ademhalings- en stofwisselingsanalyse.
-
15 april 2024
Techniek single-molecule niche in Zwaartekrachtonderzoek
Met haar expertise in single-molecule technieken gaat Dr. Kasia Tych (GBB) bijdragen aan een groot Zwaartekracht-onderzoeksprogramma
